Жесткая и мягкая вода — в чем разница
Определение 1
Жесткость воды —
Характеристики воды, связанные с количеством и типами растворенных солей щелочноземельных металлов, в основном, кальция и магния, определяют ее жесткость. Проведенные исследования показали, что присутствие двухвалентных ионов, таких как стронций, железо, марганец и барий, незначительно влияет на уровень жесткости воды, и поэтому их влиянием обычно можно пренебречь.

Вода с большим содержанием таких солей называется жесткой, с малым содержанием — мягкой. Катионо-анионный состав, определяющий жесткость, приведен в таблице 1.
Причины образования жесткой воды обусловлены вымыванием солей из пластов горных пород: известняка, гипса, доломита, которые залегают на пути водного потока.
Параметры жесткости могут меняться в зависимости от того, какие полезные ископаемые распространены в данной местности, насколько хорошо они растворимы в воде и других факторов.
Негативное воздействие жесткой воды:
- вызывает образование накипи на промышленном и бытовом водонагревательном оборудовании (в том числе в чайниках, стиральных машинах и пр.), затрудняя их работу;
- плохо образует пену;
- сушит кожу;
- увеличивает время разваривания некоторых продуктов (круп, овощей) и др.
Использование слишком мягкой воды может приводить к коррозии труб из-за отсутствия нужного кислотно-щелочного баланса, поддерживаемого гидрокарбонатами.
Вкусовые качества жесткой воды также отличаются из-за наличия или отсутствия в ней различных солей:
- повышенное содержание солей магния, особенно сульфатов, может давать горечь;
- соли железа и марганца придают воде выраженный неприятный привкус, а при кипячении еще и бурый цвет;
- хлориды определяют соленость воды.
Многим людям кажется, что мягкая вода более приятна на вкус.
В некоторых источниках встречается информация, что употребление жесткой воды приводит к таким последствиям, как образование камней в мочеполовой системе, а мягкой — увеличивает риск сердечно-сосудистых заболеваний. Однако, достоверных клинических исследований или научных докладов, подтверждающих эти сведения, пока не проводилось.
Виды жесткости воды
Виды жесткости воды и способы ее устранения приведены в таблице 1.
| Состав жесткой воды | Вид жесткости | Способы устранения | ||
| катионы | анионы | по составу | по способу устранения | |
|
Ca2+, Mg2+ (в малой степени: Fe2+и Fe3+, Mn2+, Ba2+, Sr2+,Al3+) |
HCO3- | карбонатная | временная |
|
| Cl-, SO42-, NO3- | некарбонатная | постоянная | добавление соды | |
| Cl-, SO42-, NO3- (SiO32-) | общая |
|
Таблица 1.
Кальций-ионы Са2+ отвечают за кальциевую жесткость, а магний-ионы Mg2+ — за магниевую жесткость.
У поверхностного источника по одному и тому же адресу жесткость воды может меняться в зависимости от сезона: например, весной, в период паводка, жесткость воды уменьшается. А летом вода быстро испаряется с поверхностей водоемов, особенно если мало дождей, и жесткость повышается.
В подземных источниках жесткость воды сохраняется примерно на одном, достаточно высоком уровне: 8-10 мг-экв/л.
Большой жесткостью отличается вода морей и океанов, например:
- в Черном море общая жесткость составляет 65,5 мг-экв/л, на ионы кальция приходится 12, магния — 53,5 мг-экв/л;
- в океанах средняя общая жесткость — 130,5 мг-экв/л, на ионы кальция приходится 22,5, магния — 108 мг-экв/л.
В России для водоснабжения хозяйственного и бытового назначения ГОСТ 31865–2012 устанавливает следующую норму жесткости воды: от 4 до 7 мг-экв/л. При этом питьевая вода должна содержать 2—6 мг-экв/л ионов кальция, и 1,6—3 мг-экв/л ионов магния.
В Европе, для сравнения, жесткость не должна превышать 1,2 мг-экв/л. Это значит, что европейцы привыкли пить мягкую воду.
Устранение жесткости
1. Термическая обработка: нагревание воды до 70-80 °С или кипячение позволяет почти полностью устранить временную жесткость. В процессе нагревания гидрокарбонаты распадаются с образованием угольной кислоты:
Реакция 1
а карбонат кальция и основный карбонат (или гидроксид при рН>10.3) магния выпадают в виде осадка:
Реакция 2
2. Химическая обработка.
а) Карбонатный тип жесткости можно устранить добавлением гашеной извести Ca(OH)2:
Реакция 3
б) При одновременном добавлении гашеной извести и кальцинированной соды Na2CO3 карбонатная жесткость устраняется известью, а некарбонатная — содой:
Реакция 4
Далее идет реакция с известью:
Реакция 5
MgCO3 + Ca2+ + 2OH- → Mg(OH)2↓ + CaCO3↓.
в) Применение полифосфата натрия Na5P3O10 приводит к связыванию ионов Ca2+ и Mg2+ за счет образования хорошо растворимых в воде хелатных комплексных соединений:
Реакция 6
3. Ионный обмен осуществляется с помощью ионитов — твердых веществ, имеющих подвижные ионы, которые способны замещаться ионами внешней среды. Причем обмен катионов происходит на катионы, или анионов на анионы.
Например, алюмосиликат Na2O∙Al2O3∙4SiO2∙mH2O имеет пространственную решетку, образованную атомами Al, Si и O. В ней имеются полости, в которых содержатся молекулы воды и ионы Na+. Последние могут замещаться на ионы Ca2+ и Mg2+ при пропускании воды через слой гранул алюмосиликата.
Также применяют ионообменные смолы — катиониты на основе синтетических полимеров. Их состав можно выразить общей формулой Na2R, где Na+ — подвижный катион, а R- — органический радикал с отрицательным зарядом.
При пропускании воды через слои катионита ионы кальция и магния переходят из раствора в катионит, замещая натрий:
Реакция 7
Когда процесс ионного обмена доходит до равновесия, катионит перестает выполнять свою работу. Его можно регенерировать погружением в концентрированный раствор NaCl или Na2SO4. При этом ионы Ca2+ и Mg2+ выходят в раствор, а катионит вновь насыщается ионами Na.
Рисунок 1. Принцип действия ионообменных фильтров.
Источник: filteropt.ru
4. Физические методы устранения жесткости основаны на выведении ионов кальция и магния под действием:
- электрического поля — электродиализ;
- магнитного поля;
- магнитно-ионизирующего излучения;
- ультразвуковых волн;
- обратного осмоса;
- электромагнитных волн определенной частоты.
Методы определения уровня жесткости воды
Для определения общей жесткости Жо:
1. Используется сложное комплексонометрическое титрование трилоном Б C10H14N2Na2O8. Этот метод самый точный.
Методика: 100 мл воды отбирают в коническую колбу, добавляют 5 мл аммиачно-буферной смеси, затем 7-8 капель спиртового раствора индикатора эриохрома черного Т или щепотку его сухой смеси с хлоридом натрия или калия. После перемешивания раствор окрасится в винно-красный цвет. Его титруют 0,05 н. раствором трилона Б до изменения окраски на сине-зеленую.
Формула 1
2. Покупные экспресс-тесты. Подходят для домашнего использования. Не всегда точные, зато просты в использовании и стоят недорого.
Рисунок 2. Тест-полоски для определения общей жесткости воды.
Источник: fixzip.ru
3. Измерение электропроводности с помощью кондуктометра.
Метод является приблизительным, поскольку электропроводность воды определяет не показатель жесткости, а общее содержание растворенных солей в воде, в том числе солей кальция и магния. Кондуктометр должен измерять именно удельную электропроводность, которая измеряется в мкСм/см, обычный прибор не подойдет.
Рисунок 3. График зависимости удельной электропроводности воды от ее жесткости.
Источник: m.studref.com
Для определения временной жесткости Жв в химии применяют кислотное титрование соляной кислотой.
При титровании образца воды соляной кислотой в присутствии индикатора метилового оранжевого происходит разложение бикарбонатов, обусловливающих временную жесткость:
Реакция 8
Методика определения. В лабораторную коническую колбу отбирают 100 мл исследуемой воды, добавляют 2—3 капли метилового оранжевого и титруют 0,1 н. раствором HCl до появления оранжевой окраски.
Формула 2
После определения общей и временной жесткости, рассчитывают постоянную (некарбонатную) жесткость Жп:
Формула 3
Жп = Жо — Жв.
Видео. ГОСТ 31954-2012 «Вода питьевая. Методы определения жесткости»
Современные разновидности pH-метров — pH-иономеры позволяют определять временную жесткость на основе титрования соляной кислотой, и общую жесткость с помощью комплексонометрического титрования. Кроме того, они имеют кальций-селективные электроды для различения кальциевой и магниевой жесткости.
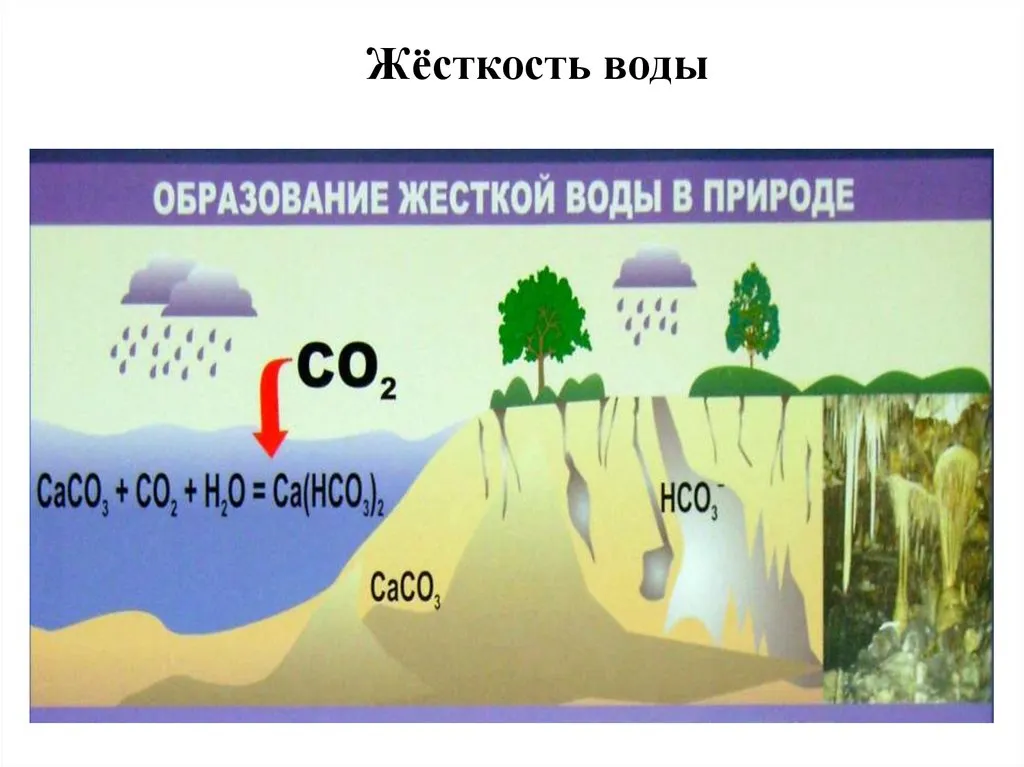
Рисунок 4. pH-иономер Metrohm 781.
Источник: donaulab.ru
Единицы измерения жесткости
Общая жесткость измеряется в градусах GH. Например, в воде, значение GH которой близко к нулю, аквариумные рыбки гибнут, употреблять ее в пищевых целях не рекомендуется.
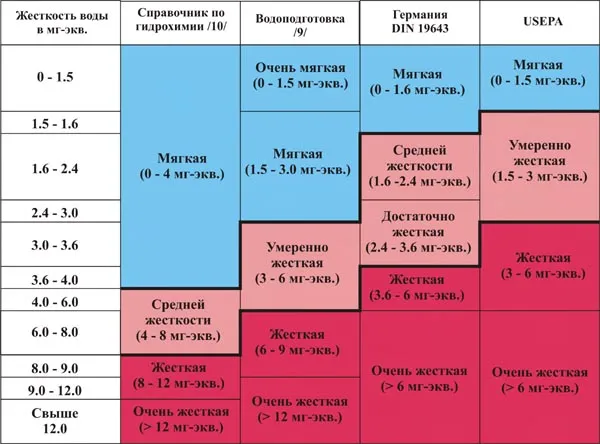
В мире для измерения параметра жесткости используются разные значения: см. рисунок 5.
Рисунок 5.
Источник: colormann.ru
С 1 января 2014 года в России действует межгосударственный стандарт ГОСТ 31865-2012 «Вода. Единица жесткости». Согласно новому ГОСТу жесткость выражается в градусах жесткости (°Ж).
2. Определение
1 °Ж соответствует концентрации щелочноземельного элемента, численно равной 1/2 миллимоля на литр (1 °Ж = 1 мг-экв/л).
По величине общей жесткости различают воду:
| Характер воды | dGH, °dH | мг-экв/л=°Ж | мг/л, ppm |
| очень жесткая | 23-34 | выше 12 | |
| жесткая | 13-22 | 8-12 | |
| средней жесткости | 9-12 | 4-8 | |
| мягкая | 5-8 | ||
| очень мягкая | 0-4 | 0-70 |
Таблица 2.
Как уменьшить жесткость воды из скважины?
Жесткость воды обычно определяется содержанием минералов, таких как кальций и магний. Высокая жесткость воды может привести к образованию накипи, ухудшению вкуса питьевой воды и другим проблемам. Существует несколько способов уменьшить жесткость воды из скважины:
-
Умягчение воды с помощью ионного обмена:
- Системы умягчения воды, основанные на ионном обмене, используют специальные смолы, которые обменивают ионы кальция и магния на ионы натрия. Это позволяет уменьшить содержание минералов, отвечающих за жесткость воды. Такие системы обычно используются в домашних условиях.
-
Добавление химических реагентов:
- Некоторые химические реагенты могут помочь осаждению минералов в нерастворимую форму, что позволит уменьшить жесткость воды. Однако этот метод может потребовать тщательного контроля и регулярного обслуживания.
-
Обратный осмос:
- Системы обратного осмоса используют полупроницаемые мембраны для удаления минералов и других загрязнений из воды. Этот метод может быть эффективным для уменьшения жесткости, но требует специального оборудования.
-
Добавление полифосфатов:
- Полифосфаты могут помочь предотвратить образование накипи и осадков, уменьшая жесткость воды. Однако этот метод может быть менее эффективным на практике.
-
Приобретение питьевой воды:
- Если жесткость воды слишком высока и другие методы неэффективны, вы можете рассмотреть возможность покупки питьевой воды с низкой жесткостью.
Перед выбором метода рекомендуется провести анализ воды из вашей скважины, чтобы определить точное содержание минералов и выбрать наиболее подходящий способ уменьшения жесткости. Лучше всего проконсультироваться с профессиональными специалистами или компаниями, специализирующимися на обработке воды, чтобы получить рекомендации и решение, наиболее подходящее для вашей ситуации.